Tóquio, 25 de fevereiro de 2026 – Pesquisadores do Earth-Life Science Institute (ELSI), vinculado ao Institute of Science Tokyo, demonstraram que determinadas enzimas podem empregar informações de reações anteriores para alterar o rumo de processos químicos, afastando-os do equilíbrio esperado. Os resultados, publicados na revista Physical Review Letters, atribuem às enzimas um papel semelhante ao “demônio de Maxwell”, conceito clássico da termodinâmica.
O grupo investigou o fenômeno conhecido como difusão enzimática aumentada (EED, na sigla em inglês), no qual moléculas enzimáticas movem-se mais rapidamente logo após catalisar uma reação. Em simulações, essa aceleração momentânea foi tratada como uma forma de “memória” física do evento catalítico.
Desvio do equilíbrio químico
Ao modelar a utilização da energia liberada na catálise para impulsionar a mobilidade da enzima, os cientistas observaram que a proporção entre substrato e produto desviou-se do ponto de equilíbrio. Sem a EED, a concentração das duas espécies químicas permanecia igual; com o aumento temporário da difusão, a quantidade de produto cresceu de modo sustentado.
Segundo o coautor Tetsuhiro S. Hatakeyama, compreender a razão física desse desvio foi o maior desafio. A chave veio quando a equipe percebeu que a enzima atuava como o demônio proposto por James Clerk Maxwell: ao “medir” o estado resultante da reação anterior (via maior mobilidade) e “feedbackar” essa informação, a molécula impedia a reação inversa e instaurava uma nova condição estacionária.
Modelo teórico e implicações biológicas
No modelo elaborado, a enzima alterna entre dois estados – normal e de alta mobilidade. A transição para o estado veloz registra o acontecimento catalítico e, enquanto dura, afasta a enzima das moléculas de produto, reduzindo a chance de reação reversa. Se a difusão intrínseca já for elevada, se o estado de alta mobilidade decair rápido demais ou se a reação inversa ocorrer antes da “fuga” da enzima, não há desvio perceptível.
Os autores destacam que parâmetros de enzimas reais, como a urease, se enquadram nas condições previstas pelo estudo, sugerindo viabilidade biológica do mecanismo. Para Kunihiko Kaneko, também coautor, a descoberta aponta que sistemas vivos podem ter explorado conversão de informação em energia desde os primórdios – hipótese que ajuda a preencher lacunas na química pré-biótica.
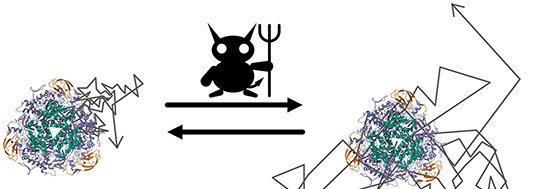
Imagem: Internet
Próximos passos
O grupo pretende investigar como o comportamento “demoníaco” das enzimas afeta redes metabólicas mais amplas dentro das células, incluindo eventuais impactos sobre o fluxo de reações e a organização espacial de metabólitos.
O estudo adiciona uma nova dimensão ao entendimento da regulação bioquímica, mostrando que enzimas não apenas aceleram reações, mas também podem direcioná-las ativamente.
Com informações de Nanowerk