Pesquisadores da Universidade de Notre Dame e da Universidade do Texas em Austin demonstraram que um único poro com largura inferior a um nanômetro, escavado em uma membrana de silício amorfo de poucos nanômetros de espessura, é capaz de “ler” a sequência de peptídeos residue a resíduo. Os resultados foram publicados em 24 de fevereiro de 2026 na revista Advanced Functional Materials.
Como funciona
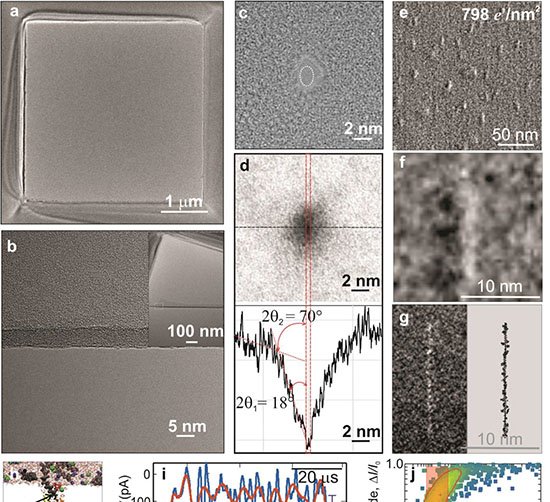
Submersa em solução salina, a membrana recebe uma diferença de potencial que faz íons atravessarem o poro gerando uma corrente elétrica estável. Quando um peptídeo entra no ponto mais estreito — cerca de 0,4 × 0,7 nm — cada aminoácido bloqueia parcialmente o fluxo iônico. A profundidade e o padrão dessas oscilações dependem do volume, da carga, da mobilidade da molécula e da água ao redor, permitindo decodificar a sequência.
Fabricação do poro
O orifício é produzido com feixe eletrônico de 300 keV em microscópio de varredura por transmissão corrigido de aberrações, sobre membranas de 3,5 a 6 nm de espessura. Após exposição ao ar, forma-se óxido nativo que estabiliza a geometria e reduz a carga superficial, criando um ambiente hidrofílico favorável à passagem das moléculas.
Preparação das amostras
Para garantir que cada resíduo passe de forma individual, os peptídeos são tratados com o detergente aniónico SDS, que os estica e lhes confere carga negativa quase uniforme. A translocação ocorre a 4 – 7 °C, temperatura que retarda o movimento e aumenta a resolução.
Prova de conceito com β-amiloide
O grupo analisou o fragmento Aβ1-42, associado ao mal de Alzheimer, e variantes clínicas, incluindo:
- mutação “Ártica” (substituição de glutamato por glicina no resíduo 22);
- glicosilação na serina 26;
- fosforilação na mesma serina.
Os dois primeiros eventos provocaram quedas claras na corrente — 2,7 e 2,5 desvios-padrão acima do ruído, respectivamente — exatamente nas posições corretas da cadeia. A fosforilação, menor em volume, ficou abaixo do limite de detecção.

Imagem: measuring how each amino acid obstructs
Coleta e análise dos sinais
A corrente foi registrada a 3,6 MHz em largura de banda de 1,8 MHz. Centenas de eventos foram agrupados por similaridade com algoritmo de propagação de afinidade; o sinal médio de cada grupo formou um “consenso” de baixa interferência. Simulações de dinâmica molecular de cada um dos 20 aminoácidos alimentaram um banco de dados para comparação. Em todos os testes, o peptídeo verdadeiro ocupou o primeiro lugar no ranqueamento.
Vantagens e limitações
O método exige apenas algumas centenas de moléculas, superando o limite mínimo de milhões de cópias do espectrometria de massas e a precisão de 28 – 61 % dos nanoporos biológicos guiados por enzimas. Contudo, ele funciona apenas com peptídeos desenovelados e ainda depende da fabricação repetível de matrizes com poros uniformes.
Segundo os autores, a combinação de confinamento extremo, medição elétrica de alta velocidade e simulações atomísticas permite localizar mutações ou modificações químicas em nível de resíduo, sinalizando um caminho para detecção de biomarcadores em concentrações ultrabaixas.
Com informações de Nanowerk