Pesquisadores do Institute of Applied Sciences and Intelligent Systems do Conselho Nacional de Pesquisas da Itália (CNR-ISASI) demonstraram que é possível escrever, apagar e reescrever campos elétricos em cristais de niobato de lítio dopado com ferro para guiar células vivas, sem necessidade de eletrodos ou contato físico. O estudo foi publicado em 27 de fevereiro de 2026 na revista Advanced Functional Materials.
Como funciona a interface biofotovoltaica
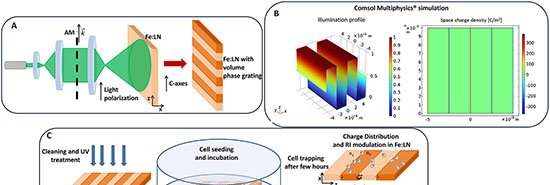
O dispositivo baseia-se no efeito fotovoltaico interno do niobato de lítio. Quando o cristal é iluminado por um laser de argônio a 514 nm, cargas se redistribuem, criando campos elétricos de até 106 V/cm dentro do material e um campo mais fraco na superfície, capaz de influenciar células aderidas.
Para programar o cristal, a equipe projetou o feixe laser através de máscaras ópticas que geram listras periódicas de 25 µm (PV-25) ou 50 µm (PV-50). O mesmo processo forma uma grade de difração interna, confirmando que o padrão de cargas foi gravado.
Testes com fibroblastos
Após a escrita dos padrões, foram semeadas células de fibroblasto de camundongo (linha NIH-3T3) em quatro substratos: PV-50, PV-25, niobato de lítio sem padrão e vidro comum. A densidade inicial de células foi igual em todas as amostras e a incubação durou 24 h.
Os resultados mostraram que cerca de 80 % das células nos cristais PV-50 e PV-25 alinharam seu eixo maior perpendicularmente às listras, seguindo o gradiente do campo elétrico. Nos substratos controle, não houve orientação preferencial. Testes estatísticos confirmaram diferença altamente significativa (ajustado p < 0,0001).
Deformação nuclear e organização do citoesqueleto
A microscopia de fluorescência revelou alterações na forma do núcleo. O índice médio de alongamento nuclear atingiu 0,5 no PV-50 e 0,4 no PV-25 (0 representa núcleo circular e 1 forma máxima alongada). Em vidro e niobato sem padrão, o índice foi 0,1. Diferenças foram significativas (p < 0,001).
Imagens confocais mostraram que filamentos de actina se reorganizaram ao longo do campo, transmitindo tensão até o envelope nuclear via complexo LINC. O espaçamento de 50 µm permitiu maior espalhamento celular dentro de cada faixa, fortalecendo a adesão e a deformação do núcleo. O período de 25 µm restringiu o espalhamento e reduziu o alinhamento.

Imagem: Nanowerk https
Controle reversível em tempo real
Microscopia holográfica digital acompanhou células vivas por 20 h e confirmou que elas permanecem confinadas às zonas ativas. Quando o padrão de cargas foi apagado com nova exposição laser, as células recuperaram mobilidade: um fibroblasto rastreado percorreu distância três vezes maior após a “borracha” óptica. Em barreiras em linha tracejada, menos de 10 % das células cruzaram o limite ativo; após o apagamento, todas migraram livremente.
Segurança e perspectivas
Testes de viabilidade apontaram sobrevivência entre 91,7 % (PV-25) e 93 % (vidro), sem diferença significativa. Atualmente, a gravação do padrão requer potências laser acima do tolerável para culturas já estabelecidas; portanto, a escrita ocorre antes da semeadura e apenas o apagamento é realizado com células presentes. O grupo trabalha para reduzir a potência de escrita e permitir reprogramação em tempo real.
Segundo os autores, a plataforma dispensa processos litográficos, fiação externa e fontes de energia contínuas, oferecendo superfície reconfigurável para engenharia de tecidos, reparo neural e estudos de migração celular.
Com informações de Nanowerk