Pesquisadores da Universidade de Groningen, na Holanda, desenvolveram um sistema capaz de entregar um medicamento dentro de células de câncer de mama triplo-negativo e, ao mesmo tempo, acompanhar em tempo real as mudanças químicas provocadas pelo tratamento.
O trabalho, descrito na revista Advanced Functional Materials, utilizou nanodiamantes fluorescentes com defeitos do tipo “vacância de nitrogênio”, estruturas que emitem luz e funcionam como sensores quânticos sensíveis a variações magnéticas e químicas.
Como funciona a plataforma
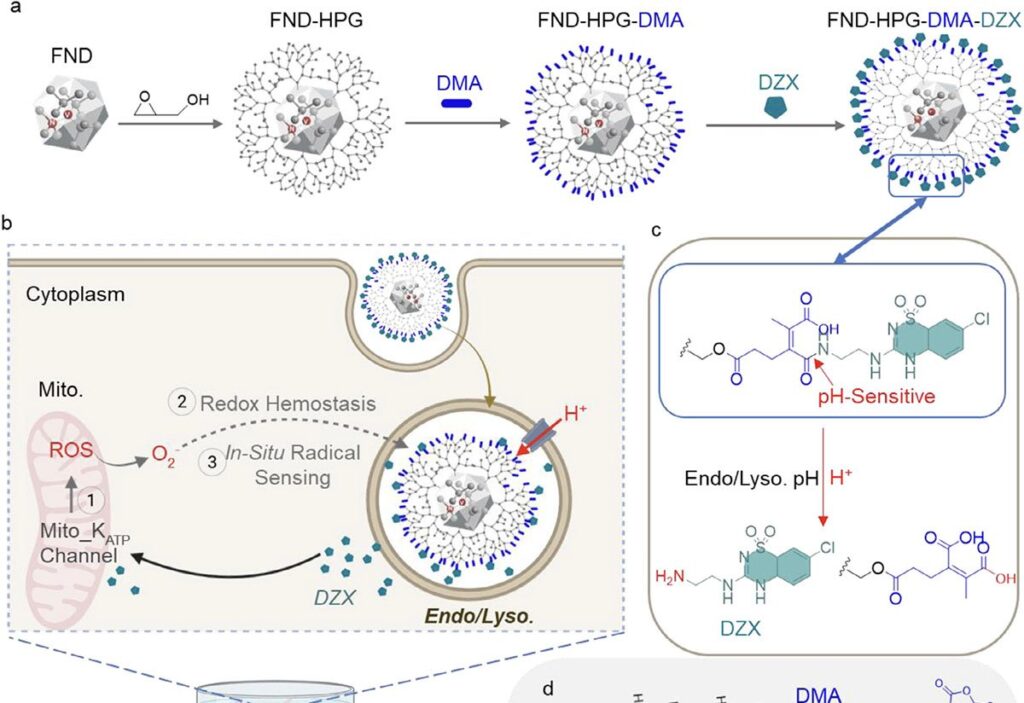
Os nanodiamantes, com menos de 100 nm de diâmetro, receberam três camadas sucessivas:
- Hiperbranched Polyglycerol (HPG), polímero que aumenta a estabilidade em meio biológico;
- Ligante sensível a pH, que mantém o fármaco preso em pH neutro e se rompe em ambiente levemente ácido;
- Diazóxido, molécula conhecida por abrir canais de potássio em mitocôndrias.
Com as modificações, o diâmetro hidrodinâmico passou de aproximadamente 120 nm para cerca de 220 nm e a carga superficial tornou-se menos negativa, favorecendo a entrada nas células.
Liberação controlada do fármaco
Testes em tampão ácido (pH 6,5) mostraram que cerca de 80 % do diazóxido é liberado em oito horas; em pH 7,4, apenas 25 % se desprende no mesmo período. O processo segue cinética de primeira ordem.
Experimentos em células
Em cultivos de células MDA-MB-231 (câncer de mama triplo-negativo), as nanopartículas concentraram-se inicialmente em lisossomos. A dose aplicada correspondeu a 2,75 µM de diazóxido, nível que preservou a viabilidade celular.
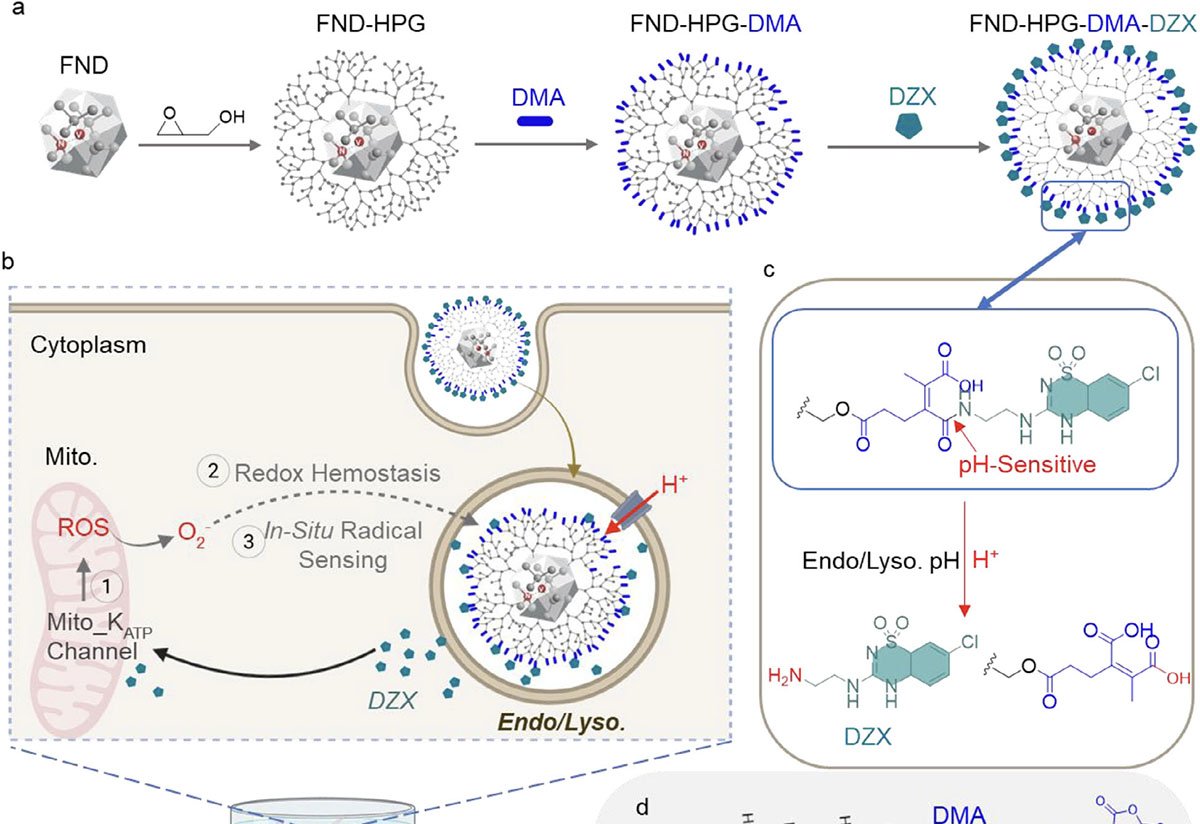
Imagem: chical stress through their quantum li
Após a liberação do fármaco, os próprios nanodiamantes registraram alterações na quantidade de radicais livres por meio de relaxometria T1. Em 24 h, o tempo T1 aumentou no citoplasma e em lisossomos, indicando queda local de radicais, enquanto a produção de espécies reativas de oxigênio subiu nas mitocôndrias. Aos 48 h, os valores citoplasmáticos voltaram ao normal, mas o estresse mitocondrial persistiu.
Três funções em uma única partícula
O estudo demonstra a integração de: liberação controlada por pH, rastreamento óptico e detecção quântica de mudanças redox. Segundo os autores, a combinação permite observar onde o fármaco age e como altera a química celular sem destruir a amostra — um avanço para terapias guiadas por feedback em tempo real.
Entre os desafios futuros estão reduzir o tamanho final das partículas, aumentar a estabilidade em altas concentrações e adaptar a técnica para tecidos mais espessos ou modelos animais.
Com informações de Nanowerk