Uma equipe do Laboratório de Tecnologias Avançadas de Fabricação da Escola de Engenharia da EPFL, na Suíça, apresentou o MEDS (Magnetic Endoluminal Deposition System), primeiro bioprinter ingerível capaz de ser guiado pelo trato gastrointestinal para depositar bio-tinta sobre áreas lesionadas. O estudo foi publicado em 16 de outubro de 2025 na revista Advanced Science.
Como funciona
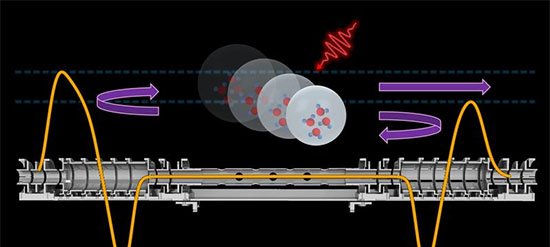
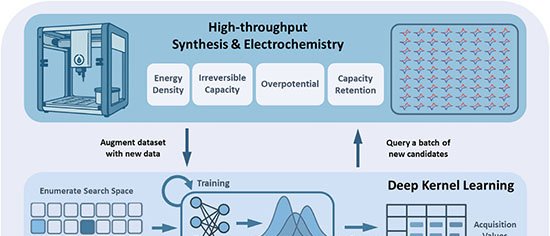
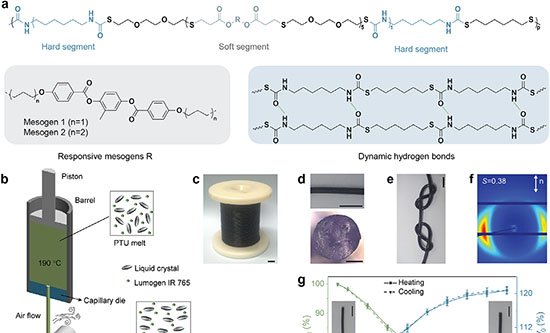
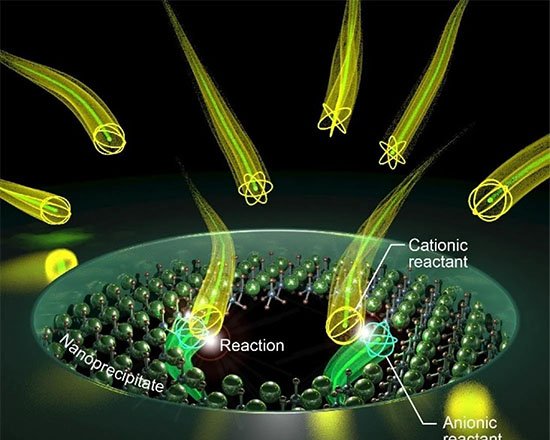
Com dimensões semelhantes às de um comprimido, o MEDS guarda uma câmara de bio-tinta — gel biocompatível feito a partir de polímeros naturais — e um mecanismo de êmbolo acionado por mola. A liberação do material é ativada por um feixe de laser infravermelho próximo que atravessa com segurança os tecidos corporais. Enquanto a tinta sai, a cápsula é orientada por um ímã externo acoplado a um braço robótico, permitindo precisão no depósito, segundo os pesquisadores.
Resultados em laboratório e testes in vivo
Nos experimentos, o dispositivo reparou úlceras artificiais de diferentes tamanhos e vedou um sangramento simulado em tecido gástrico sintético. Em seguida, em testes realizados em coelhos em um centro de pesquisa credenciado nos Estados Unidos, a equipe conseguiu posicionar a bio-tinta no estômago dos animais, acompanhando todo o trajeto via fluoroscopia por raio X. Após o procedimento, a cápsula pôde ser removida pela boca utilizando magnetismo, reduzindo a necessidade de intervenções invasivas.
Potencial terapêutico
De acordo com o coordenador do laboratório, Vivek Subramanian, o MEDS une conceitos de bioprintagem in situ com as cápsulas inteligentes já usadas para liberação de fármacos, inaugurando uma nova categoria de dispositivos médicos não invasivos. Já o doutorando Sanjay Manoharan destacou que, em ambiente controlado, a bio-tinta carregada com células manteve integridade estrutural por mais de 16 dias, funcionando como microbiorreator capaz de liberar fatores de crescimento e atrair novas células para o local da lesão.

Imagem: Internet
Os autores afirmam que os próximos passos incluem adaptar a tecnologia para atuação em vasos sanguíneos e nos tecidos da parede abdominal (peritônio). Eles também planejam validar a eficácia do método em estudos adicionais em animais antes de avançar para testes clínicos.
Com informações de Nanowerk