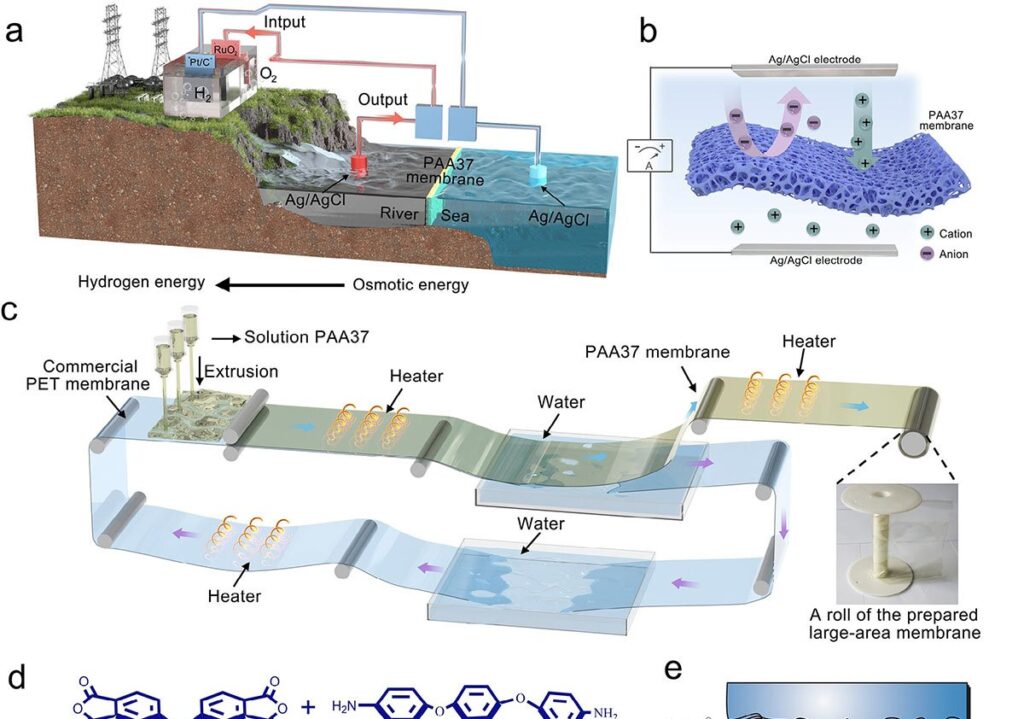
Pesquisadores apresentaram um sistema que transforma o encontro entre água doce e água salgada em energia elétrica suficiente para alimentar a eletrólise da água, produzindo hidrogênio de forma contínua e sem necessidade de corrente externa. O estudo, publicado em 20 de outubro de 2025 na revista Advanced Materials, combina uma pilha de osmose reversa com um eletrolisador comercial.
Como funciona
No coração do dispositivo está a membrana polimérica PAA37, um poliácido amídico rico em grupos carboxila. Esses grupos conferem carga negativa aos nano-canais do filme, atraindo quase exclusivamente íons positivos e bloqueando os negativos. O número de transferência cátionica (t) alcançou 0,96, próximo do seletivo ideal (1,0).
Ao expor a membrana a uma diferença de concentração de 50 para 1 (0,01 M contra 0,5 M de cloreto de potássio), o sistema gerou tensão de circuito aberto de 176 mV — 96 % do valor teórico para esse gradiente. Um único módulo com área ativa de 3,14 mm² atingiu densidade de potência de 6 W/m² em temperatura elevada.
Escala e durabilidade
A PAA37 foi produzida por polimerização e secagem em processo roll-to-roll, permitindo rolos de 450 cm × 20 cm (9 000 cm²) e resistência à tração de 63 MPa, além de baixa absorção de água. Em testes de bancada, a membrana funcionou durante cinco dias sob gradiente salino antes de apresentar fissuras superficiais, indicando necessidade de reforço mecânico.
Desafio do dimensionamento
Ao aumentar a área da membrana, a equipe comprovou, por meio da chamada equação HLZ, que a maior parte das perdas elétricas ocorre no eletrodo do lado de água doce, onde a condutividade iônica é menor. Reduzir a impedância desse eletrodo e encurtar a distância até a membrana são caminhos apontados para manter o desempenho em escala maior.
Integração com eletrólise
Uma pilha de 110 módulos conectados em série gerou 24,34 V, mas a alta resistência interna reduziu a tensão disponível no eletrólisador para 0,8 V. Reorganizando-se o arranjo em cinco ramais paralelos de 22 módulos em série cada, a tensão entregue subiu para 1,51 V, suficiente para iniciar e sustentar a produção visível de hidrogênio. A eficiência de conversão — fração da energia osmótica teórica transformada em potência elétrica útil — chegou a 42 %.
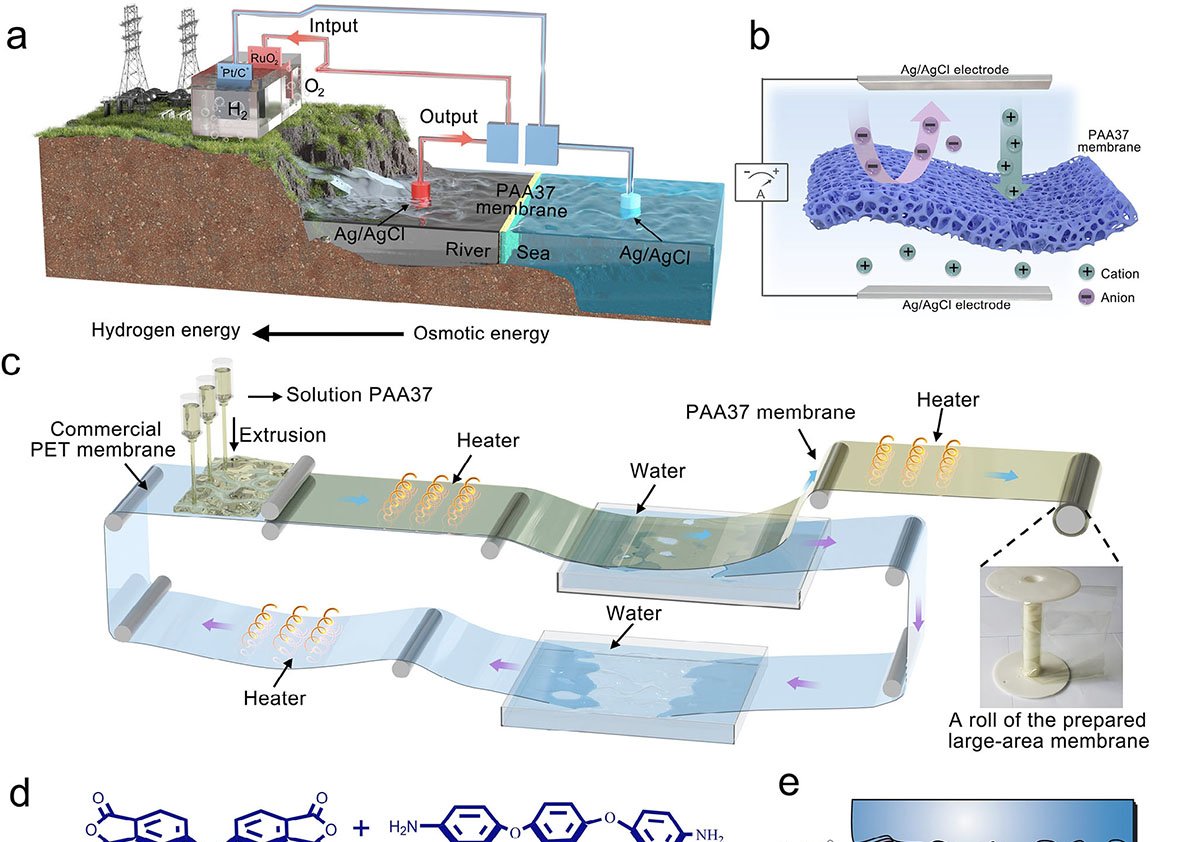
Imagem: improving how these mbranes are arrang
Os autores sugerem que, em instalações reais, o fluxo contínuo de água doce de rios e de água salgada do mar manteria o gradiente salino estável, evitando a queda de tensão observada no sistema fechado de laboratório.
O trabalho demonstra que diferenças naturais de salinidade podem gerar energia elétrica estável para eletrólise, aproximando a chamada “energia azul” de uma rota prática para a produção limpa de hidrogênio.
Com informações de Nanowerk