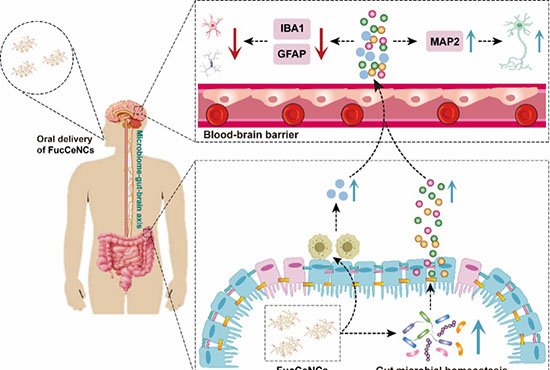
Pesquisadores liderados pela Universidade de Macau demonstraram, pela primeira vez, a síntese de estruturas cristalinas porosas – os covalent organic frameworks (COFs) – diretamente dentro de células vivas. O trabalho, publicado em 26 de fevereiro de 2026 na revista Advanced Materials, mostra que a formação dessas redes dentro dos lisossomos causa a ruptura dessas organelas, libera ferro e desencadeia ferroptose, um tipo de morte celular dependente de ferro. Em modelos murinos, o processo reduziu tumores e ativou respostas imunológicas sistêmicas.
Como o COF é montado no interior celular
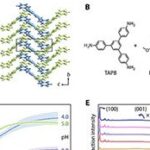
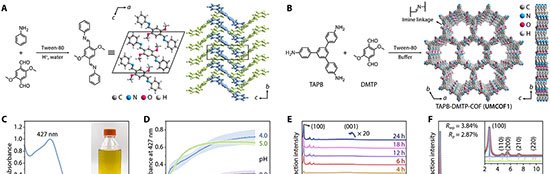
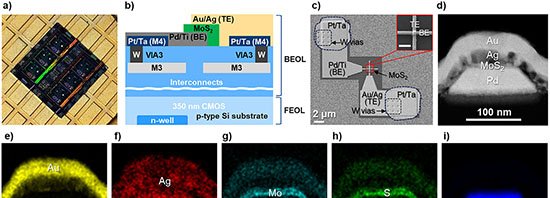
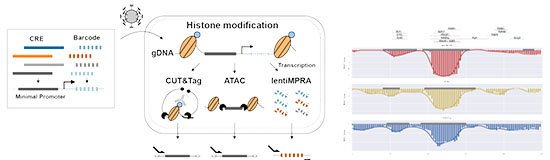
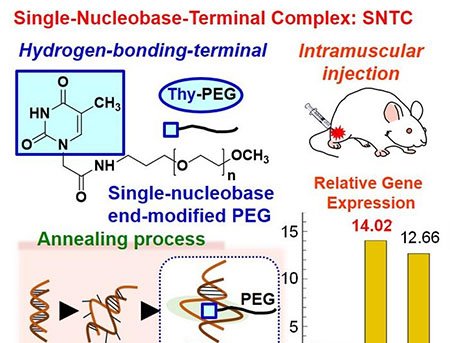
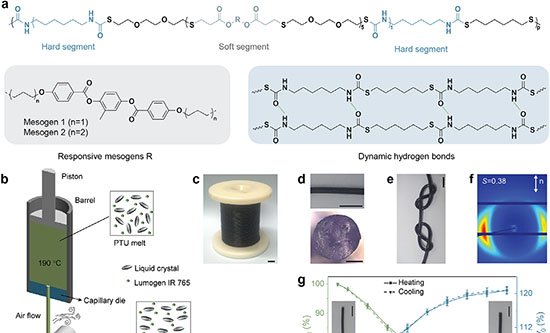
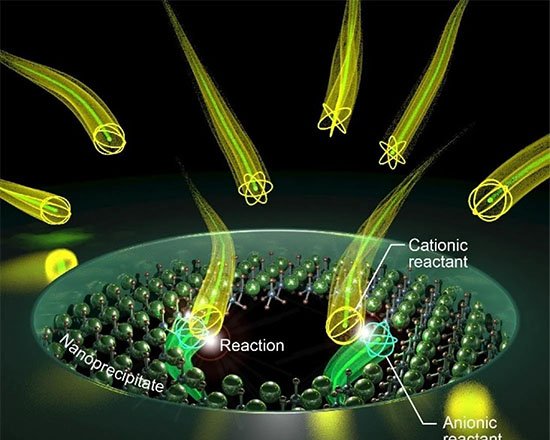
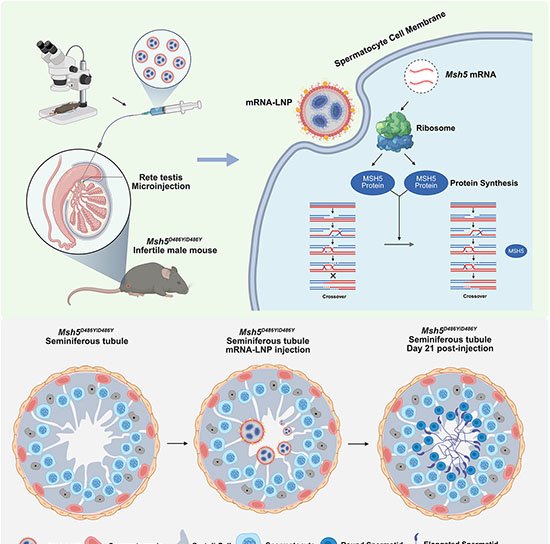
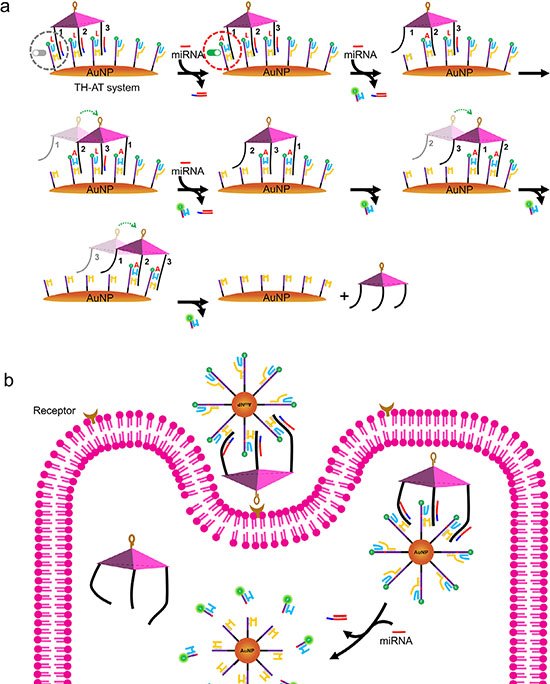
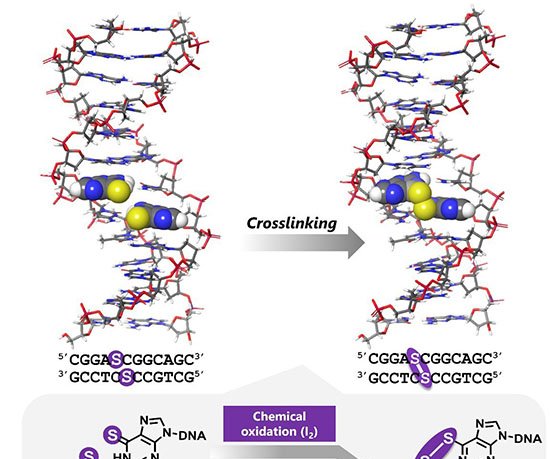
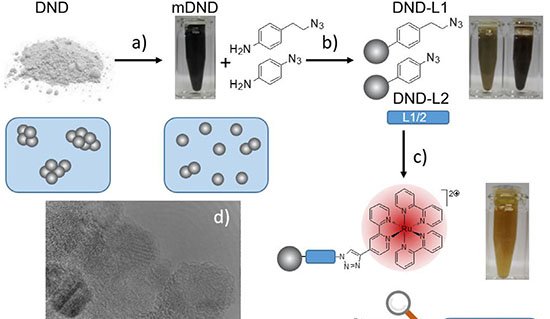
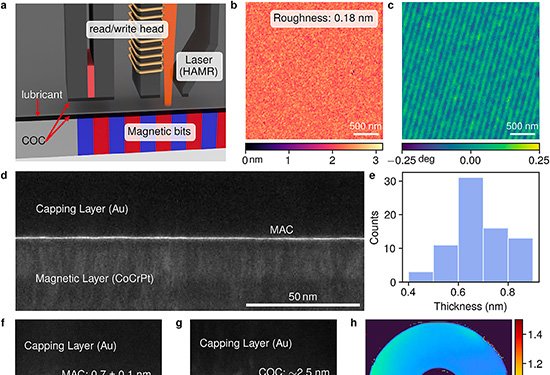
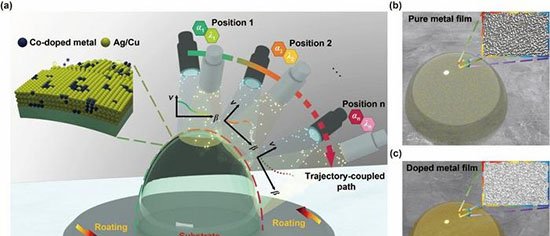
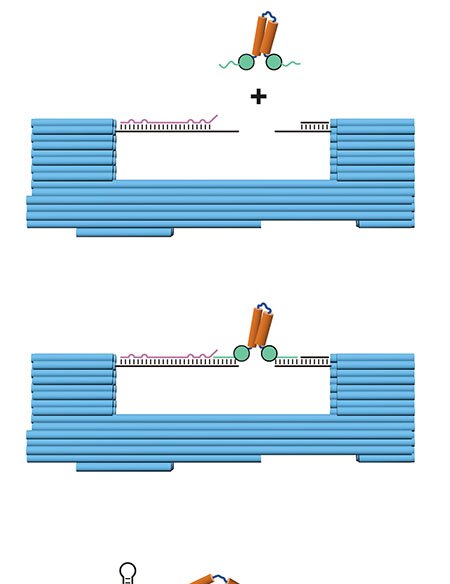
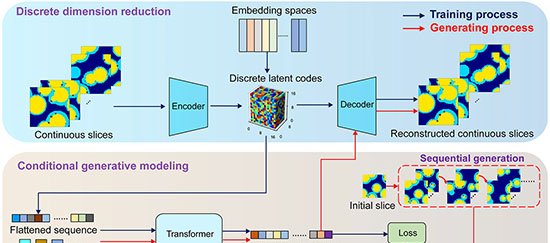
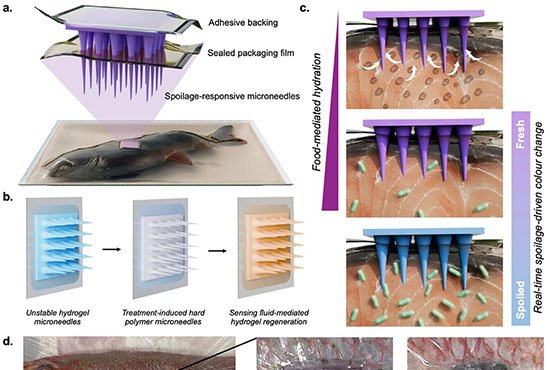
O grupo utilizou dois monômeros pequenos – TAPB (triamina) e DMTP (dialdeído) – que entram na célula e se acumulam em lisossomos, cuja acidez natural (pH 4,5–5,0) catalisa a condensação de imina. Em tampão fosfato a 37 °C, na presença do surfactante Tween-80, os monômeros cristalizam em um COF batizado de UMCOF1. Fora da célula, a reação atinge equilíbrio em seis horas e gera um pó amarelo insolúvel com rendimento de 76 %.
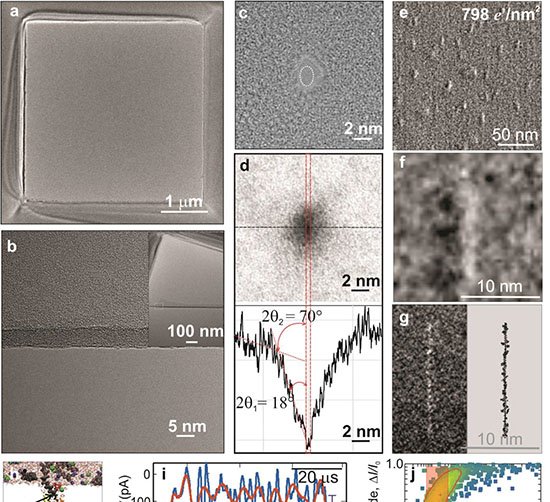
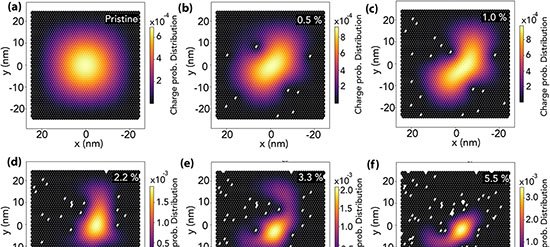
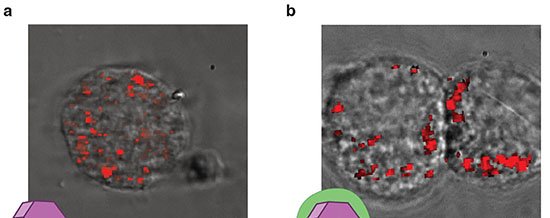
Dentro das 4T1, linhagem de câncer de mama murino, a formação de UMCOF1 foi rastreada por fluorescência verde (excitação a 405 nm). Quando a acidez lisossomal foi neutralizada com bafilomicina A1, o sinal caiu para 28 %, confirmando a dependência do ambiente ácido. Microscopia eletrônica identificou nanopartículas esféricas de cerca de 120 nm e difração de raios X de material extraído comprovou a ordem atômica do polímero.
Ferroptose e ativação imune
A montagem do COF rompeu a membrana lisossomal, liberando ferro que catalisa peroxidação lipídica. A concentração de TAPB que matou 50 % das células foi de 44,3 µM. Inibidores de ferroptose e o quelante deferoxamina anularam o efeito, enquanto monômeros isolados ou COF pré-sintetizado, adicionados externamente, não foram tóxicos.
Comparado ao indutor de ferroptose RSL3, o COF liberou sinais de perigo (ATP e HMGB1) de forma mais lenta e constante e expôs calreticulina na superfície celular, marcando as células para fagocitose. Supernatantes de células tratadas com COF ativaram macrófagos e promoveram a liberação de citocinas inflamatórias; o mesmo não ocorreu com RSL3.
Resultados em animais
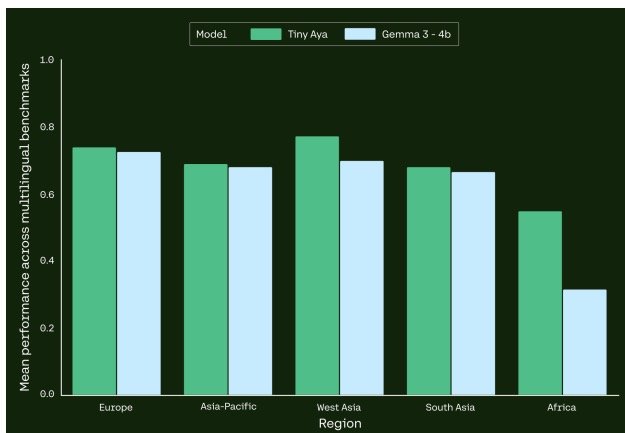
Em camundongos com tumores 4T1, a injeção intratumoral dos dois monômeros reduziu o peso tumoral para 19 % do controle após 15 dias, sem perda de peso corporal ou toxicidade orgânica detectável. Macrófagos M1 aumentaram 6,6 vezes, células dendríticas maduras quase cinco vezes e a proporção de linfócitos T CD8⁺/CD4⁺ subiu significativamente.

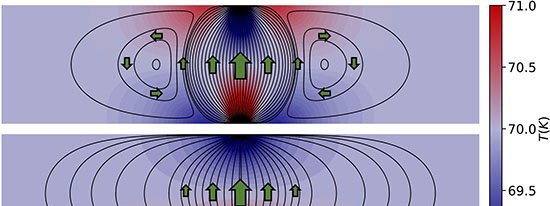
Imagem: lipid damage
Ao ser combinado com o agonista imune R848, o tratamento também inibiu tumores distantes não injetados, demonstrando efeito abscopal. Uma vacina preparada com lisados de células tratadas retardou o aparecimento de tumores em camundongos imunocompetentes; metade deles permaneceu livre da doença, enquanto animais deficientes em linfócitos T não apresentaram proteção.
Limitações apontadas
Os autores admitem que a estratégia não diferencia células normais de tumorais in vitro, exigindo métodos de direcionamento para uso sistêmico. Além disso, o destino a longo prazo dos monômeros fora do sítio tumoral ainda não foi investigado.
Com informações de Nanowerk