19 de fevereiro de 2026 – Pesquisadores da Universidade da Califórnia em Santa Barbara (UCSB) apresentaram uma técnica que facilita a produção de aminoácidos não naturais já habilitados para a montagem de peptídeos, ampliando drasticamente as opções disponíveis além dos 22 tipos encontrados na natureza.
O que há de novo
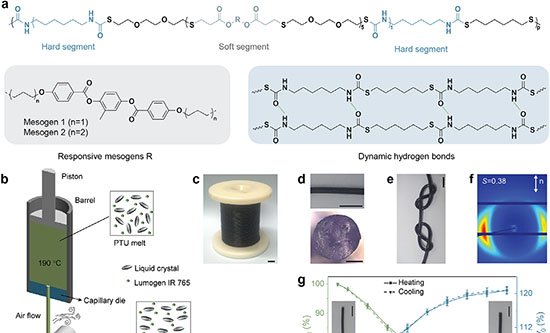
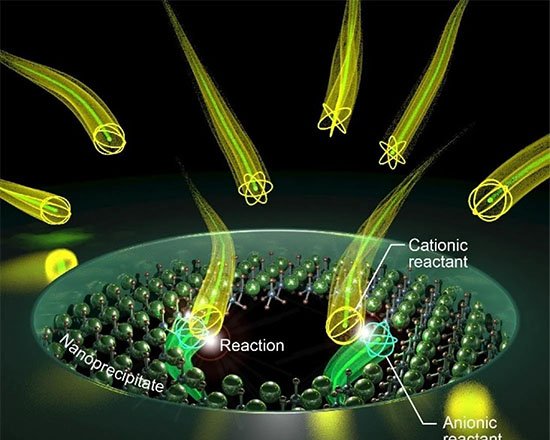
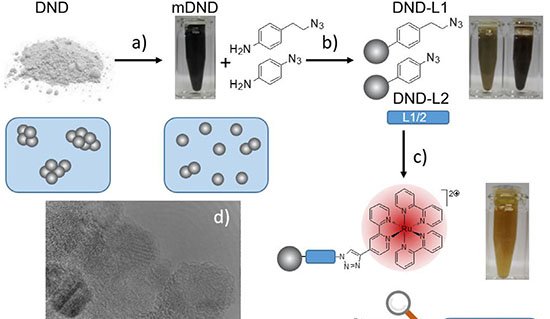
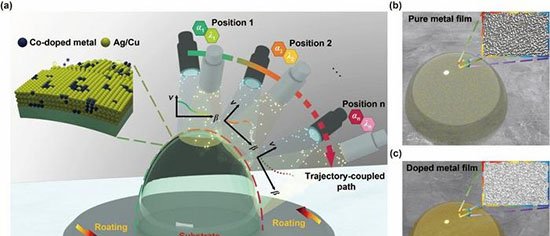
O procedimento, descrito na Journal of the American Chemical Society sob o título “Expedient Synthesis of N-Protected/C-Activated Unnatural Amino Acids for Direct Peptide Synthesis”, utiliza catálise à base de ouro para gerar aminoácidos a partir de insumos químicos de baixo custo. Esses compostos saem da reação com o grupo ácido ativado, exigindo apenas a remoção de uma proteção no grupo amino antes de se unirem em cadeia.
Quem está por trás
A pesquisa é assinada pelo doutorando Phil Kohnke, primeiro autor, e orientada pelo professor Liming Zhang, ambos do Departamento de Química e Bioquímica da UCSB.
Como funciona
Em duas etapas, o time produz os aminoácidos e, em seguida, utiliza um suporte de resina para ligar as unidades, adicionando-as uma a uma num ciclo de enxágue e repetição. O processo é altamente estereosseletivo, gerando apenas a forma desejada (mão direita ou esquerda) do aminoácido e simplificando a purificação: ao final, o peptídeo é clivado da resina e lavado.
Por que importa
Com acesso a um leque mais amplo de blocos de construção, químicos, biomédicos e cientistas de materiais podem criar peptídeos mais estáveis ou moldados para se ligar com precisão a seus alvos biológicos. Medicamentos como o Ozempic, usado contra diabetes e obesidade, já incorporam aminoácidos não naturais para aumentar eficácia e durabilidade.

Imagem: Internet
Próximos passos
A equipe trabalha na automação da técnica e busca parcerias para torná-la acessível a laboratórios focados em desenvolvimento de fármacos e novos materiais.
Com informações de Nanowerk